- 產(chǎn)地
- 蘇州
- 品牌
- 外泌體提取試劑
- 型號
- 齊全
- 是否定制
- 是
外泌體的提取主要包括以下幾種方式。一是超速離心法,這是目前外泌體提取較常用的方法。此種方法得到的外泌體量多,但是純度不足,電鏡鑒定時發(fā)現(xiàn)外泌體聚集成塊,由于微泡和外泌體沒有非常統(tǒng)一的鑒定標準,也有一些研究認為此種方法得到的是微泡不是外泌體。二是過濾離心,這種操作簡單、省時,不影響外泌體的生物活性,但同樣存在純度不足的問題。三是密度梯度離心法,用此種方法分離到的外泌體純度高,但是前期準備工作繁雜,耗時,量少。外泌體檢測作為一種新型的液體活檢熱點技術(shù)已被許多臨床科研機構(gòu)普遍地應(yīng)用于一些病癥和疾病的無創(chuàng)診斷外泌體提純試劑盒的特色與優(yōu)勢:樣本輸入量多樣。貴陽正規(guī)外泌體提取試劑直銷價

外泌體與肺病預(yù)后:外泌體mirRNA和蛋白質(zhì)被認為是NSCLC的預(yù)后因子。Dejima等在研究NSCLC患者預(yù)后的生物標志物時發(fā)現(xiàn),外泌體miR-4257和miR-21的含量顯著上升。此外,還有研究表明,低水平miR-146a-5p的NSCLC患者較高水平miR-146a-5p的NSCLC患者有更高的復(fù)發(fā)率。Sandfeld-Paulsen等在研究276例NSCLC患者血漿的外泌體時發(fā)現(xiàn),NY-ESO-1是其中對低生存率有顯著影響的標志物。Silva等利用TaqMan低密度芯片的方法系統(tǒng)分析了28位NSCLC患者體內(nèi)的365種miRNA,其中l(wèi)et-7f、miR-30e-3p和miR-20b表達均下調(diào),進一步研究發(fā)現(xiàn)。武漢正規(guī)外泌體提取試劑廠家直銷外泌體提取:低速離心去除細胞和凋亡碎片。

專利申請利用分離培養(yǎng)人尿液來源細胞并收集培養(yǎng)基來進行體外培養(yǎng),直接把外泌體從尿液中沉降下來,無須分離培養(yǎng)人尿液來源細胞并收集培養(yǎng)基。人尿液來源細胞的外泌體的獲取方法,是首先分離培養(yǎng)人尿液來源細胞并收集培養(yǎng)基,將人尿液來源細胞的培養(yǎng)基通過0.22微米濾膜過濾,以去除大的細胞殘片以及其它雜質(zhì);然后離心除去細胞器,留取上清;再使用可截留100KD分子量的膜,通過離心截留上清中的外泌體,截留完成后,使用PBS對膜進行洗脫即得到外泌體濃縮液。
外泌體的生物學(xué)功能研究中需要分離完整的外泌體顆粒,而傳統(tǒng)超速離心方法步驟繁瑣、硬件要求高、操作難度大。李記生物自主開發(fā)的外泌體快速提取試劑盒,組分經(jīng)過優(yōu)化處理,適用于細胞培養(yǎng)上清液、血清、血漿、尿液及其他體液(腦脊液、腹水、羊水、乳汁以及唾液等)中的外泌體提取,并搭配純化過濾裝置,可快速高效地獲得高純度外泌體顆粒。注意事項:1.對于待測樣品粘度過大時,可將樣本用4℃預(yù)冷的1×PBS緩沖液進行等體積稀釋處理。2.當血清、血漿、唾液等樣品收獲的外泌體濃度較高,收獲的外泌體顆粒無法通過EPF柱純化時,可用4℃預(yù)冷的1×PBS進行稀釋后再通過EPF柱離心。重復(fù)離心操作還有可能對囊泡造成損害,從而降低其質(zhì)量。
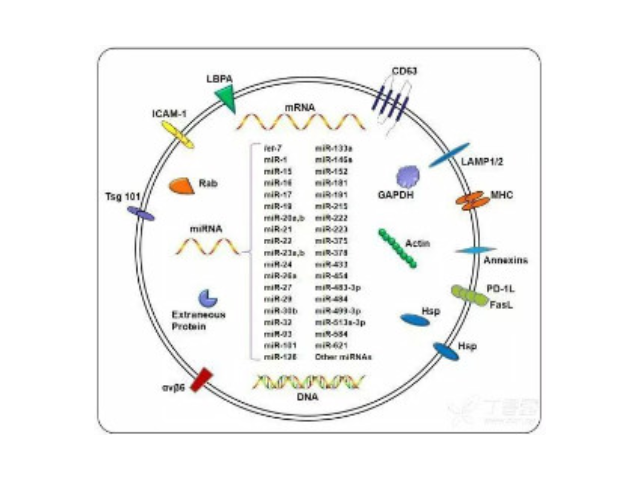
外泌體項目獲批學(xué)科方向:從統(tǒng)計來看,與前年相似外泌體立項集中的領(lǐng)域還是一些病癥學(xué),近年來外泌體發(fā)表的文章也絕大部分與其在一些病癥的形成,耐藥性,檢測等方面有關(guān)。例如2019年發(fā)表在MolecularCancer(IF=10.679)上的文章表明外泌體FMR1-AS1通過TLR7/NFκB/c-My信號通路在女性食管ai中促進維持ai癥干細胞樣細胞的動態(tài)平衡。發(fā)表在JournalofExperimental&ClinicalCancerResearch(IF=5.646)上的一篇文章發(fā)現(xiàn)外泌體轉(zhuǎn)運p-STAT3可促進結(jié)直腸ai細胞獲得性5-FU耐藥性。發(fā)表在Cancers(IF=6.162)上的一篇文章則研究了腹腔灌洗液中細胞外囊泡相關(guān)的miRNA作為子宮內(nèi)膜ai分子標志物的可能性。此外,在神經(jīng)系統(tǒng)和精神疾病,中醫(yī)學(xué)及其他領(lǐng)域也有不少外泌體相關(guān)項目中標。外泌體:形成了一種全新的細胞間信息傳遞系統(tǒng),影響細胞的生理狀態(tài)并與多種疾病的發(fā)生與進程密切相關(guān)。寧波外泌體提取試劑產(chǎn)品介紹
用無菌針管吸取上層含有外泌體的液體,置于80℃儲存?zhèn)溆谩YF陽正規(guī)外泌體提取試劑直銷價
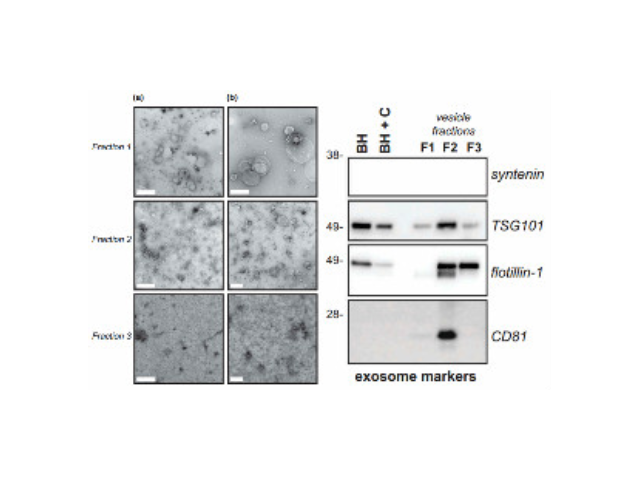
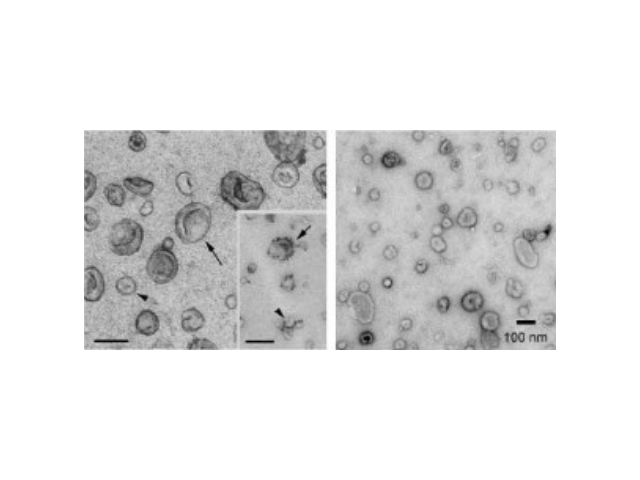
外泌體(Exosomes)是細胞分泌到胞外的一種囊泡(ExtracellularVesicles,EVs),其大小為30-150nm,具有雙層膜結(jié)構(gòu)和茶托狀形態(tài),含有豐富的內(nèi)含物(包括核酸、蛋白和脂質(zhì)等),參與細胞間的分子傳遞。外泌體普遍存在于細胞培養(yǎng)上清以及各種體液中,包括血液、唾液、尿液、乳汁等,同時也存在于組織樣本中,如腦組織、肌肉組織、脂肪組織等。腦組織分離方法簡述:將腦組織剪成薄片,放入離心管中加上消化液進行消化,經(jīng)水浴、反復(fù)輕輕上下顛倒,再用移液間斷緩慢吹吸至消化結(jié)束。隨后加入培養(yǎng)基于消化液中,混勻,置于冰上。再進行一系列的差速超速離心過程,包括除雜、濾膜過濾、超離等。較后用PBS重懸外泌體,用重懸后的外泌體進行下面的透射電鏡(TEM)、納米粒徑追蹤分子(NTA)和markerWB鑒定。來源于細胞內(nèi)溶酶體微粒內(nèi)陷形成的多囊泡體,經(jīng)多囊泡體外膜與細胞膜融合后釋放到胞外基質(zhì)中。貴陽正規(guī)外泌體提取試劑直銷價
外泌體相關(guān)miRNA與肺病的診斷:miRNAs是一類含有20~25個核苷酸的非編碼小RNA,能夠通過下調(diào)或壓制靶mRNAs來調(diào)節(jié)轉(zhuǎn)錄水平上的基因表達,目前非編碼RNA被普遍發(fā)現(xiàn)存在于NSCLC患者外泌體中,參與一些病癥的形成和演化過程。單個miRNA可能通過壓制性復(fù)合物與多個mRNA結(jié)合,從而阻滯整個生物通路。因此,外泌體的miRNA具有成為NSCLC標志物的優(yōu)勢。Chen等在152例肺病患者的研究中初次報道了循環(huán)游離miRNA的表達,與75例健康者相比,發(fā)現(xiàn)了兩種高表達的miRNA(miR-25和miR-223)。Rabinonowits等對27例肺病患者和9例健康人的血漿外泌體中12個mi...
- 蕪湖正規(guī)外泌體提取試劑哪里買 2025-08-26
- 長沙外泌體提取試劑報價 2025-08-26
- 石家莊正規(guī)外泌體提取試劑直銷廠家 2025-08-26
- 開封正規(guī)外泌體提取試劑廠家推薦 2025-08-26
- 深圳外泌體提取試劑產(chǎn)品介紹 2025-08-26
- 重慶正規(guī)外泌體提取試劑廠家現(xiàn)貨 2025-08-26
- 廈門正規(guī)外泌體提取試劑直銷價 2025-08-26
- 杭州外泌體提取試劑報價 2025-08-25
- 廣州外泌體提取試劑哪里買 2025-08-25
- 昆明正規(guī)外泌體提取試劑生產(chǎn)廠家 2025-08-25
- 武漢正規(guī)外泌體提取試劑哪家好 2025-08-25
- 杭州正規(guī)外泌體提取試劑廠家供應(yīng) 2025-08-25
- 貴陽外泌體提取試劑產(chǎn)品介紹 2025-08-24
- 武漢外泌體提取試劑廠家批發(fā)價 2025-08-24
- 唐山外泌體提取試劑廠家現(xiàn)貨 2025-08-24
- 合肥正規(guī)外泌體提取試劑推薦廠家 2025-08-24


- 溫州細胞外基質(zhì)膠 08-26
- 金華正規(guī)細胞外基質(zhì)膠價格 08-26
- 鄭州細胞外基質(zhì)膠廠家批發(fā)價 08-26
- 石家莊正規(guī)外泌體提取試劑直銷廠家 08-26
- 青島細胞外基質(zhì)膠直銷價 08-26
- 開封正規(guī)外泌體提取試劑廠家推薦 08-26
- 深圳外泌體提取試劑產(chǎn)品介紹 08-26
- 蘇州細胞外基質(zhì)膠廠家現(xiàn)貨 08-26
- 貴陽正規(guī)細胞外基質(zhì)膠廠家批發(fā)價 08-26
- 南京細胞外基質(zhì)膠單價 08-26